Лечение умеренного когнитивного дефицита: Диагностика и лечение умеренных когнитивных нарушений в пожилом возрасте
Синдром умеренных когнитивных расстройств в пожилом возрасте: диагностика и лечение | Захаров В.В., Яхно Н.Н.
Умеренные когнитивные расстройства (УКР) представляют собой относительно новый термин, который все чаще встречается в современной неврологической и гериатрической литературе. Под данным термином принято понимать нарушения памяти и других высших мозговых функций, как правило, у пожилого человека, которые выходят за рамки возрастной нормы, но не приводят к социальной дезадаптации, то есть не вызывают деменцию [13,22,23,35–38].
Термин «умеренные когнитивные расстройства» (англ.: mild cognitive impairment) был включен в Десятый пересмотр международной классификации болезни, как самостоятельная диагностическая позиция. Согласно рекомендациям МКБ–10, данный диагноз может быть выставлен при наличии следующих условий [6]:
• снижение памяти, внимания или способности к обучению;
• жалобы пациента на повышенную утомляемость при выполнении умственной работы;
• нарушения памяти и других высших мозговых функций не вызывают деменцию и не связаны с делирием;
• указанные расстройства имеют органическую природу.
Умеренные когнитивные расстройства по определению не связаны только с возрастными изменениями головного мозга или с дисметаболическими расстройствами, вторичными по отношению к соматическим заболеваниям или экзогенным интоксикациям. Данный термин также не приложим к психогенным когнитивньм нарушениям в рамках депрессии или других психических расстройств, не имеющих известной органической природы.
В отечественной литературе английский термин «mild cognitive impairment» иногда переводится также как «легкое когнитивное расстройство», «мягкое когнитивное расстройство» или «мягкое когнитивное снижение». Мы полагаем, что наиболее точным эквивалентом английского термина является выражение «умеренные когнитивные расстройства», так как оно в большей мере соответствует нормам русского языка и подчеркивает значимость обсуждаемой проблемы.
Эпидемиология УКР
Распространенность синдрома УКР среди пожилых лиц требует дальнейшего уточнения. В настоящее данные о встречаемости этого синдрома, базируются, в основном, на результатах двух широких эпидемиологических исследований: Канадского Исследования Здоровья при Старении (Canadian Study of Health and Aging, 1997) и Итальянского Лонгитудинального Исследования Старения (Italian Longitudinal Study of Aging, 2000). В цитируемых исследованиях было получено, что когнитивные нарушения, которые выходят за пределы возрастной нормы, но не достигают выраженности деменции, отмечаются у 11–17% пожилых и старых людей. Риск развития синдрома УКР в возрасте старше 65 лет в течение одного года составляет 5%, а за 4 года наблюдения – 19%. При этом в большинстве случаев синдром УКР является прогрессирующим состоянием. У 15% пациентов с синдромом УКР в течение одного года развивается деменция, что достоверно чаще, чем в общей популяции пожилых лиц. За 4 года наблюдения 55–70% случаев УКР трансформируется в деменцию [18,23,24,26].
Приведенные эпидемиологические данные подчеркивают важность клинического распознавания синдрома УКР в пожилом возрасте. Очевидно, что деменция развивается на развернутых стадиях заболеваний головного мозга, когда возможности компенсации существенно ослаблены. Ранняя диагностика церебральных заболеваний, на стадии додементных когнитивных нарушений, существенно увеличивает шансы на успешность терапевтических мероприятий. Таким образом, практическая значимость разработки концепции умеренных когнитивных расстройств в пожилом возрасте заключается в привлечении внимания врачей и исследователей к более ранним стадиям прогрессирующих церебральных заболеваний, разработка диагностических и терапевтических алгоритмов ведения больных с начальными симптомами мнестико–интеллектуальной недостаточности с целью предотвращения или замедления наступления деменции [7].
Этиология и патогенез
Как и деменция, умеренные когнитивные расстройства являются полиэтиологическим синдромом, который может развиваться в рамках широкого спектра неврологических заболеваний. Однако клинико–морфологические сопоставления свидетельствуют, что чаще всего клиническому диагнозу синдрома УКР соответствуют патологоанатомические маркеры нейродегенеративного процесса и сосудистой мозговой недостаточности [22,23]. Как клинические наблюдения, так и фундаментальные исследования последних лет неоспоримо свидетельствуют, что два названных патологических процесса тесно взаимосвязаны на патогенетическом уровне. Существуют веские доказательства того, что хроническая церебральная ишемия способствует более раннему началу и более быстрому прогрессированию нейродегенеративного процесса. С другой стороны, при наиболее распространенных нейродегенеративных заболеваниях, таких как болезнь Альцгеймера (БА) и деменция с тельцами Леви, развитие хронической ишемии глубинных отделов белого вещества головного мозга является закономерным. Среди патогенетических механизмов последнего обсуждается амилоидная ангиопатия и эпизоды падения артериального давления, связанные с вегетативной недостаточностью. Таким образом, в большинстве случаев когнитивные нарушения в пожилом возрасте, вероятно, носят смешанный сосудисто–дегенеративный характер [1,14,28,30,37].
Хотя, как уже говорилось выше, умеренные когнитивные нарушения в пожилом возрасте по определению связаны не только со старением, нельзя недооценивать вклад собственно возрастных изменений головного мозга в когнитивную дисфункцию у пожилого человека. Известно, что с возрастом уменьшается общая масса головного мозга, меняются морфофункциональные свойства церебральных сосудов, снижается активность нейротрансмиттерных систем головного мозга. В частности, отмечается значительное уменьшение дофаминергической медиации, что, возможно, лежит в основе некоторых существенных симптомов возрастной когнитивной дисфункции [10,15,33].
Основные клинические
проявления синдрома УКР
Синдром УКР характеризуется клинической полиморфностью, которая отражает патогенетическую разнородность данного состояния. Чаще всего на первый план выходит прогрессирующее ухудшение памяти (по P. Petersen – «амнестический тип УКР»). Данный тип нарушений обычно является предвестником развернутой картины БА [34,35,36]. Другая распространенная форма нейродегенеративного процесса – деменция с тельцами Леви – обычно дебютирует с нарушений зрительно–пространственного восприятия [11]. Для сосудистой мозговой недостаточности и заболеваний с преимущественным поражением базальных ганглиев более характерны интеллектуальная инертность, брадифрения и снижение концентрации внимания [5,9]. В клинической картине фронто–темпоральной дегенерации обычно преобладают поведенческие расстройства, связанные со снижением критики. В редких случаях клиническая картина синдрома УКР характеризуется преобладанием речевых или диспрактических нарушений. Такие расстройства характеризуют начальные стадии первичной прогрессирующей афазии и кортико–базальной дегенерации соответственно [34,35,36]. Когнитивные нарушения при синдроме УКР, как правило, сочетаются с другими психическими расстройствами (эмоциональными, поведенческими) и неврологическими симптомами. Характер данных симптомов также зависит от нозологической формы УКР.
Диагноз
и дифференциальный диагноз
Диагностика синдрома УКР базируется на субъективных жалобах пациента на снижении памяти и умственной работоспособности и на данных объективных методов исследования. Для объективизации когнитивных нарушений широко используются нейропсихологические методы. При этом набор нейропсихологических методик должен быть достаточно простым, чтобы обеспечить диагностику синдрома УКР на этапе первичного неврологического консультирования, но в то же время достаточно чувствительным к относительно небольшим по выраженности когнитивньм расстройствам.
Следует отметить, что в настоящее время нет общепринятого методического инструмента для нейропсихологической диагностики синдрома УКР. Большинство рекомендуемых тестов, такие как тест слухо–речевой памяти Рея, тест избирательного напоминания Бушке, «логическая память» Векслеровской шкалы памяти и другие, являются в значительной степени трудоемкими и требуют не менее 15–30 минут для проведения и интерпретации [23]. Поэтому в клинической практике обычно применяются более простые методики, хорошо зарекомендовавшие себя в скрининговой диагностике деменции. Речь идет о краткой шкале исследования психического статуса (англ. – Mini–Mental State Examination) и тесте рисования часов [5,20,30]. Однако чувствительность данных нейропсихологических методик на этапе УКР далеко не всегда достаточна. Поэтому для уточнения диагноза нередко бывает необходимо динамическое наблюдение за пациентом и повторные клинико–психологические исследования. Нарастание выраженности когнитивных нарушений со временем является одним из наиболее надежных признаков патологического характера когнитивных расстройств. Важно отметить, что при нормальном старении снижение памяти и других когнитивных способностей носит практически стационарный характер [5,13,27].
Для дифференциального диагноза между физиологической возрастной когнитивной дисфункцией и начальными признаками патологического ухудшения высших мозговых функций существенное значение имеет анализ характера нарушений памяти. Результативность мнестических тестов снижается как при нормальном старении, так и при различных нейрогериатрических заболеваниях. Так, при болезни Альцгеймера, которая развивается у 5–15% пожилых лиц, нарушение памяти обычно является самым первым симптомом заболевания. Однако механизмы возрастного и патологического ухудшения памяти различны. При нормальном старении забывчивость связана преимущественно со снижением активности запоминания и воспроизведения, в то время как первичные механизмы памяти остаются сохранными. В отличие от этого при болезни Альцгеймера нарушается сама способность усвоения новой информации. Поэтому внешняя организация процесса запоминания в сочетании с подсказками при воспроизведении в значительной степени компенсирует возрастную забывчивость, но малоэффективна при болезни Альцгеймера, в том числе на ранних ее стадиях. Эти данные легли в основу метода дифференциального диагноза нормального и патологического старения, впервые предложенного Гробером и Бушке [17,25]. В настоящее время методический принцип, разработанный указанными авторами, используется в тесте «5 слов» [19].
Помимо нейропсихологических тестов, для диагностики синдрома УКР широко используются клинические шкалы, которые содержат описания наиболее типичных когнитивных, поведенческих и функциональных симптомов, характерных для ранних стадий БА и других нейрогериатрических заболеваний. К числу таких шкал относятся клиническая рейтинговая шкала деменции (КРШД) (англ. clinical dementia rating) и общая шкала нарушений (ОШН) (англ. global deterioration scale) [31,39]. Принято считать, что описание «сомнительной деменции» по КРШД и стадии «легких» нарушений по ОШН соответствует синдрому УКР (см. приложения 1 и 2).
Диагноз УКР является, по существу, синдромальным. Констатация наличия когнитивных расстройств, выходящих за пределы возрастной нормы, недостаточна для понимания природы заболевания и выработки терапевтической тактики. Поэтому пациенты с синдромом УКР подлежат тщательному клиническому и инструментальному обследованию с целью выявления возможной причины нарушений: начальных признаков нейродегенеративного процесса, сосудистой мозговой недостаточности, других неврологических заболеваний. При этом о возможной начинающейся болезни Альцгеймера будет свидетельствовать преобладание в клинической картине нарушений памяти, быстро прогрессирующий характер расстройств, отсутствие очаговой неврологической симптоматики, атрофия гиппокампа при МРТ головного мозга [1,5,28,30]. В пользу сосудистой мозговой недостаточности говорят связь нарушений с перенесенными инсультами, наличие очаговой неврологической симптоматики, а также постишемических кист и выраженных изменений белого вещества при МРТ головного мозга [1,5,9]. Другие заболевания с картиной УКР имеют свои специфические черты и особенности психического и неврологического статуса.
Важным этапом дифференциального диагноза синдрома УКР является исключение вторичного характера когнитивных нарушений по отношению к системным метаболическим расстройствам. Пациенты с синдромом УКР требуют полноценного исследования соматического статуса и биохимического скрининга крови [13]. Другой причиной «вторичных» когнитивных расстройств являются эмоциональные нарушения. Подозрение на наличие депрессии у пациента с когнитивными расстройствами требует назначения антидепрессантов ex juvantibus. Однако при этом следует избегать препаратов с выраженным холинолитическим эффектом, например, трициклических антидепрессантов, так как данные препараты могут негативно влиять на высшие мозговые функции. Напротив, современные антидепрессанты из группы селективных ингибиторов обратного захвата серотонина (пароксетин, флуоксетин, флувоксамин и др.) благоприятно воздействуют на когнитивные функции [13,23].
Фармакотерапия синдрома УКР
Лечение пациентов с синдромом УКР должно быть индивидуальным и направленным на те патогенетические факторы нарушений когнитивных функций, которые определяются при клиническом и инструментальном исследовании в каждом конкретном случае. Ниже будут коротко освещены основные группы фармакологических препаратов, которые могут применяться при наиболее частых патогенетических вариантах синдрома УКР, связанных с начинающейся болезнью Альцгеймера, сосудистой мозговой недостаточностью или сочетанием обоих патогенетических факторов.
Ингибиторы ацетилхолинэстеразы (реминил, ривастигмин) являются препаратами первого выбора для лечения болезни Альцгеймера. Применение данных препаратов основывается на хорошо известных фактах о роли ацетилхолинергической медиации в процессах памяти и внимания. Сегодня эффективность ингибиторов ацетилхолинэстеразы имеет весьма авторитетную доказательную базу при легкой и умеренной деменции, связанной с БА [1,4,5,29]. Активно изучается также эффективность данных препаратов при сосудистой и смешанной деменции [1,2]. Обсуждаются перспективы их применения на этапе УКР [23]. Теоретически, чем раньше будут назначены ингибиторы ацетилхолинэстеразы, тем больше ожидаемый эффект. Однако учитывая фармакоэкономические аспекты терапии ингибиторами ацетилхолинэстеразы, возможность системных побочных эффектов, их назначение целесообразно лишь при полной уверенности врача в патологическом характере расстройств и в нозологическом диагнозе, что не всегда достижимо при легкой выраженности когнитивных нарушений на стадии УКР.
Антагонисты NMDA–рецепторов к глутамату оказывают симптоматический ноотропный эффект и, по экспериментальным данньм, обладают нейропротекторньм действием при болезни Альцгеймера, сосудистой и смешанной деменции [12,41]. Положительный эффект антагонистов NMDA–рецепторов связан с уменьшением нейротоксичности глутамата. Избыточная активность глутаматергической системы наблюдается как при нейродегенеративном процессе, так и при ишемии головного мозга, и играет важную патогенетическую роль в процессах повреждения нейронов. Как и в отношении ингибиторов ацетилхолинэстеразы, применение антагонистов NMDA–рецепторов при синдроме УКР теоретически оправдано, но не имеет пока надежной доказательной базы.
Как при нейродегенеративном процессе, так и при сосудистой мозговой недостаточности патогенетически оправданным является воздействие на микроциркуляцию. Вазоактивные препараты весьма широко назначаются в отечественной неврологической практике при жалобах на снижение памяти в пожилом возрасте [4,5]. Данные препараты хорошо переносятся и, по мнению большинства клиницистов, оказывают значимый ноотропный эффект. Однако требования доказательной медицины требуют повторного исследования их эффективности при строгом соблюдении диагностических критериев УКР. В отношении некоторых из указанных препаратов такие исследования в настоящее время активно проводятся. Открытым остается вопрос о длительности применения вазоактивных препаратов. В отечественной практике они традиционно назначаются курсами по 2–3 месяца 1–2 раза в год. Однако учитывая то, что синдром УКР знаменует собой определенные стадии хронического прогрессирующего заболевания головного мозга, вероятно, с патогенетических позиций более оправданным является длительное, возможно, постоянное применение данных препаратов.
С целью воздействия преимущественно на связанные с возрастными изменениями когнитивные симптомы могут применяться дофаминергические препараты. Результаты недавних исследований с применением методов функциональной нейровизуализации свидетельствуют о роли дофаминергической недостаточности в формировании возрастной когнитивной дисфункции [15,33]. Эти данные могут служить основанием для применения дофаминергических препаратов как при значительной выраженности физиологических возрастных изменений когнитивных функций, так и у пожилых лиц с патологическом синдромом УКР [З]. Эффективность агониста дофаминовых рецепторов пронорана при синдроме УКР недавно была показана в контролируемом клиническом испытании D. Nagaraja и соавт. [32].
Весьма перспективньм является применение в терапии когнитивных нарушений в пожилом возрасте пепдидергического препарата церебролизина. Данный препарат представляет собой продукт ферментативного расщепления головного мозга свиней и состоит из низкомолеклярных пептидов и свободных аминокислот. Результаты многочисленных экспериментальных исследований свидетельствуют, что церебролизин оказывает неспецифическое многомодальное положительное воздействие на нейрональный метаболизм и процессы пластичности нейронов. Поэтому данный препарат может применяться как при нейродегенеративном процессе, так и при сосудистой мозговой недостаточности и возрастных изменениях когнитивных функций.
Патогенетически обоснованным является также применение церебролизина в восстановительном периоде инсульта и черепно–мозговой травмы [1,4].
К настоящему времени накоплен значительный клинический опыт применения церебролизина. Данный препарат успешно используется для лечения когнитивных расстройств различной этиологии и инсульта в нашей стране и за рубежом на протяжении более 40 лет [8]. Эффективность церебролизина была доказана в серии контролируемых клинических испытаний с применением двойного слепого метода исследования. Так, недавно были опубликованы результаты международного исследования, проводившегося на базе центров в Канаде, Германии и Южной Корее [16,21,40]. Было показано, что церебролизин оказывает положительный эффект в отношении когнитивных функций при болезни Альцгеймера с легкой и умеренной выраженностью деменции, который сохранялся в течение, по меньшей мере, 5 месяцев после проведенного курса лечения. По мнению С. Вае и соавт., ноотропный эффект церебролизина при БА не уступает эффекту ингибиторов ацетилхолинэстеразы [16].
Таким образом, всестороннее клинико–инструментальное исследование пожилых лиц с жалобами на снижение памяти позволяет выявить когнитивные нарушения и установить нозологический диагноз еще до развития клинически очерченной деменции. Это имеет большое практическое значение, поскольку в распоряжении неврологов в настоящее время имеются возможности эффективной терапии когнитивных нарушений в пожилом возрасте. При этом более ранняя диагностика и более раннее начало терапии значительно повышают шансы на успех лечения. Активное изучение патогенеза нейрогериатрических заболеваний в настоящее время дает основания ожидать разработки в недалеком будущем способов предотвращения развития деменции при диагностике нарушений начале патогенетической терапии на этапе синдрома УКР.
Приложение 1.
Общая Шкала Нарушений.
III стадия: Легкие когнитивные нарушения.
Reisberg В., Ferris S.H., de Leon M.J et al. The global deterioration scale for assessment of primary degenerative dementia. //Am J Psychiatry. –1982. –V.I 39.–P. 1136–1139
По крайней мере два из следующих признаков:
• Нарушения ориентировки в незнакомой местности
• Снижение профессиональной компетентности, заметное для сослуживцев
• Трудности подбора слова при разговоре
• Невозможность пересказать прочитанное
• Трудности запоминания имен новых знакомых
• Трудности отыскания вещей из–за снижения памяти о том, «что куда положил»
• Нарушения серийного счета
Объективные признаки когнитивной недостаточности могут быть получены только при детальном нейропсихологическом исследовании.
Когнитивные нарушения приводят к снижению профессиональной и социальной компетентности.
Отрицание становится механизмом психологической защиты.
Когнитивные нарушения сопровождаются симптомами тревоги от легкой до умеренной выраженности.
Приложение 2.
Клинический Рейтинг Деменции.
Стадия 0,5: Сомнительная деменция
Morris J.C. The Clinical Dementia Rating (CDR): current version and scoring rules. //Neurology. – 1993. – V. 43. – P. 2412–2414.
ПАМЯТЬ: неполное припоминание событий
ОРИЕНТИРОВКА: сохранена, но могут быть неточности при назывании даты
ИНТЕЛЛЕКТ: незначительные трудности при решении сложных задач, анализе сходств и различий, не затрагивающих повседневную жизнь
СОЦИАЛЬНОЕ ВЗАИМОДЕЙСТВИЕ: незначительные трудности при сохранной независимости
БЫТ: незначительные трудности
САМООБСЛУЖИВАНИЕ: не нарушено
Список литературы Вы можете найти на сайте http://www.rmj.ru
Литература:
I .Дамулин И.В. Болезнь Альцгеймера и сосудистая деменция. //Под ред. Н.Н.Яхно. –М.–2002. –С.85.
2. Дамулин И.В. Терапевтические возможности при болезни Альцгеймера и сосудистой деменции. //Русский медицинский журнал. –2001. –Т.9. № 7–8.
З. Захаров В.В., Локшина А.Б. Применение препарата проноран (пирибедил) при легких когнитивных расстройствах у пожилых больных с дисциркуляторной энцефалопатией. //Неврологический журнал. –2004. –Т.9. № 2. –С.30–35.
4. Захаров В.В., Дамулин И.В., Яхно Н.Н. Медикаментозная терапия деменции. //Клиническая фармакология и терапия. –1994. –Т.З. –№ 4. –С.69–75.
5. 3ахаров В.В., Яхно Н.Н. Нарушения памяти. //Москва: ГеотарМед. –2003. –С.150.
6. Международная статистическая классификация болезней и проблем, связанных со здоровьем. Десятый пересмотр. (МКБ–10). // –Женева, ВОЗ. –1995. –С.317.
7. Яхно Н.Н., И.В.Дамулин, В.В.Захаров, О.С–Левин, М.Н.Елкин. Опыт применения высоких доз церебролизина при сосудистой деменции. //Тер Архив. –1996. –Т.68. –№ 10. –С.65–69.
8. Яхно Н.Н. Актуальные вопросы нейрогериатрии. //В сб.: «Достижения в нейрогериатрии). Н.Н.Яхно, И.ВДамулин (ред). –Москва: ММА им. И.М.Сеченова. –1995. –С.9–29.
9. Яхно. Н.Н., Левин О.С., Дамулин И.В. Сопоставление клинических и МРТ–данных при дисциркуляторной энцефалопатии. Сообщение 2: когнитивные нарушения. //Неврол.журн. –2001. –Т.6. –№.3. –С. 10.
10. Яхно Н. Н., Лавров А. Ю. Изменения центральной нервной системы при старении // Нейродегенеративные болезни и старение (Руководство для врачей) / Под ред. И. А. Завалишина,Н. Н. Яхно, С И Гавриловой. – М, 200!. – С. 242 – 261
11. .Яхно Н.Н., Преображенская И.С, Деменция с тельцами Леви. //Неврологический журнал. –2003 –Т 8 –№ 6 –С .4–1!
12. Яхно Н.Н., Дам1р^1н И.В., Преображенская И.С., Мхитарян Э.А. Ьолезнь Альцгеймера ‘ir деменция с тельцами Леви: некоторые аспекты клиники диагностики и лечения. //Русский медицинский журнал. –2003. –1.11. –№.100.
13. Яхно Н.Н., Захаров В.В. Легкие когнитивные расстройства в пожилом возрасте. //Неврологический журнал. –2004. –Т.9. № 1. –С.4–8.
14. XVII Всемирный неврологический конгресс. Сообщение 1 //Неврологический журнал.–2002.–1.7.–№1.–С.53–61.
15. Backman L, Ginovart N.. Dixon R et a! Age–related cognitive deficits mediated hv changes in the striatai dopamine system. //Am J Psychiatry. –2000. –V.I 57. –P.635–637.
1б. Вае C.Y., Cho C.Y., Cho K. et al. A double blind, placebo–controlled multicenter study of Cerebrolysin in Alzheimer’s disease. //J Am Geriatr Soc. –2000. –V.48. –P. 1566–1571.
17. Bushke H, E.Grober. Genuine memory deficit in age associated memory impaiment. //DevNeuropsychol. –1986. –V. 2. –P.287–307.
18. .DiCarlo A., Baldereschi M., Amaducci L. Et al. Cognitive impairment without dementia in older people: prevalence, vascular risk factors, impact on disability. The Italian Longitudinal Study on Aging. //J Am Ger Soc. –2000. –V.48. –P.775–782.
19. Dubois В., Touchon J., Portet F. et al. The 5–word test: a simple and sensitive test for me diagnosis of Alzheimer’s disease. //Paris. –2002. –P.19.
20. Folstein M.F., S.E.Folstein, P–R–McHugh. Mini–Mental State : a practical guidefor grading the mental state of patients for me clinician. J Psych Res, 1975, V.12, pp 189–198.
21. Gauthier S. Results of a 6–month randomized placebo–controlled study w
.
Лечение легких и умеренных когнитивных нарушений | Яхно Н.Н., Захаров В.В.
Когнитивные нарушения представляют собой одно из наиболее распространенных проявлений органического поражения головного мозга. В прошлом основной акцент в изучении и лечении когнитивных расстройств делался в отношении деменции. Однако развитие методов диагностики и лечения недостаточности когнитивных функций в последние годы привели к значительному повышению интереса к проблеме недементных (легких и умеренных) когнитивных нарушений (табл. 1) [13].
Как из видно из таблицы 1, умеренные когнитивные нарушения (англ. – mild cognitive impairment, MCI) представляют собой моно– или полифункциональные когнитивные расстройства, которые явно выходят за рамки возрастной нормы, но не ограничивают самостоятельность и независимость, то есть не вызывают дезадаптации в повседневной жизни. Распространенность умеренных когнитивных нарушений (УКН) среди пожилых лиц, по данным популяционных исследований, достигает 12–17%. Среди неврологических пациентов синдром УКН встречается в 44% случаев («ПРОМЕТЕЙ», 2005) [7,16,18,26].
При легких когнитивных нарушениях показатели психометрических шкал могут оставаться в пределах среднестатистической возрастной нормы или отклоняться от нее незначительно. Тем не менее больные осознают снижение когнитивных способностей по сравнению с преморбидным уровнем и выражают свое беспокойство по этому поводу. Риск прогрессирования легких когнитивных расстройств и их трансформации в умеренные и тяжелые у таких пациентов выше среднестатистического. Популяционные исследования распространенности легких когнитивных нарушений до настоящего времени не проводилось. Однако можно предположить, что их распространенность не уступает распространенности умеренных когнитивных нарушений [13].
Лечение легких и умеренных когнитивных нарушений преследует две основные цели:
– вторичная профилактика деменции, замедление темпа прогрессирования когнитивных расстройств;
– уменьшение выраженности уже имеющихся нарушений с целью улучшения качества жизни пациентов и их родственников.
Лечение, в идеале, должно быть направленным на причину нарушений, то есть быть этиотропным или патогенетическим. При этом следует учитывать высокую коморбидность гериатрических заболеваний. По статистике, большинство пожилых лиц одновременно страдают несколькими неврологическими и/или соматическими заболеваниями. В частности, весьма велик процент сосуществования сосудистой мозговой недостаточности и первичного дегенеративного поражения головного мозга. Так, на стадии деменции клинические и морфологические признаки сочетанного (сосудистого и дегенеративного) поражения головного мозга определяются в 48–73% случаев [15,17,19,20,25]. Поэтому полноценное ведение пациентов с когнитивными расстройствами включает всестороннюю оценку как психо–неврологического, так и соматического статуса, коррекцию имеющихся дисметаболических нарушений, сосудистых факторов риска, лечение депрессии, применение антиоксидантов, вазоактивных, метаболических и нейротрансмиттерных препаратов.
Коррекция дисметаболических
нарушений
По статистике, не менее 5% деменций в пожилом возрасте вызываются системными дисметаболическими расстройствами, которые связаны с соматическими или эндокринными заболеваниями, дефицитарными состояниями. Еще не менее чем в 30% случаев имеется сочетание первичного органического поражения головного мозга и дисметаболических нарушений. Наиболее распространенными в клинической практике дисметаболическими состояниями, которые отрицательно влияют на когнитивные функции, являются гипотиреоз, печеночная и почечная энцефалопатия, дефицит витамина В12 и фолиевой кислоты, хроническая гипоксия, сердечно–легочная недостаточность, экзогенные интоксикации, в том числе лекарственные (холинолитики, бензодиазепины, нейролептики и др.) [3,4,6].
Примерный перечень необходимых клинических и инструментальных обследований у пациентов с когнитивными нарушениями перечислен в таблице 2. Важно отметить, что в случае своевременной диагностики и полной коррекции, когнитивные нарушения дисметаболической природы являются полностью обратимыми.
Коррекция сосудистых
факторов риска
Артериальная гипертензия, атеросклероз церебральных артерий и другие сердечно–сосудистые заболевания являются важнейшими факторами риска возникновения и прогрессирования когнитивных нарушений в пожилом возрасте. Сегодня патогенетическое значение сосудистых факторов риска доказано не только в отношении собственного цереброваскулярного поражения, но и дегенеративного процесса, в том числе болезни Альцгеймера (БА). Исходя из такого представления терапевтическое воздействие на сосудистые факторы риска являются составной частью патогенетической терапии в большинстве случаев когнитивных расстройств в пожилом возрасте [3,4,6,24].
К концу ХХ века в мире было выполнено 5 крупномасштабных рандомизированных международных исследований различных антигипертензивных средств, в которых оценивались различные аспекты их эффективности, в том числе влияние на когнитивные функции (табл. 3). Профилактический эффект в отношении прогрессирования когнитивных расстройств и возникновения деменции был показан у кальциевого блокатора нитрендипина и при использовании комбинации периндоприла и индапамида. Есть также данные о положительном эффекте блокатора рецепторов к ангиотензину–II эпросартана [27].
Следует оговориться, что нормализации артериального давления следует добиваться планомерно и постепенно. Длительная артериальная гипертензия ведет к изменению реактивности церебральных сосудов и нарушению механизмов ауторегуляции мозгового кровотока. В этих условиях быстрое снижение привычных для больного цифр артериального давления может приводить к усугублению церебральной гипоперфузии, возникновению острых нарушений мозгового кровообращения и хронической ишемии мозга. Особенно опасно выраженное и быстрое снижение артериального давления при наличии гемодинамически значимого атеросклероза магистральных артерий головы.
Большой интерес вызывает перспектива использования гиполипидемических препаратов из группы статинов для профилактики когнитивных расстройств в пожилом возрасте. Предполагается, что применение статинов обосновано как при сосудистом поражении головного мозга, так и при БА. В последнем случае препараты данной фармакологической группы могут вмешиваться и замедлять процессы амилоидогенеза, которые являются ключевыми в патогенезе БА, причем данный эффект не зависит от снижения уровня холестерина в сыворотке крови. Однако в ходе рандомизированных контролируемых исследований, выполненных на сегодняшний день, не было показано, что длительное применение правастатина и симвастатина способствует уменьшению заболеваемости деменцией или уменьшению темпа прогрессирования когнитивных расстройств (исследования PROSPER и Heart Protection Study) [27].
Неоспоримо значение адекватной терапии других сердечно–сосудистых заболеваний, в частности, нарушений сердечного ритма. Вероятно, благоприятным эффектом в отношении сердечно–сосудистой системы обусловлено снижение риска возникновения когнитивных нарушений у лиц, регулярно выполняющих физические упражнения.
Лечение депрессии
Депрессия является весьма распространенным эмоциональным расстройством в пожилом возрасте. Депрессия у пожилого человека может быть как ситуационно обусловленной, так и иметь органическую природу. В первом случае частыми причинами депрессии являются изменения социального статуса, утрата близких родственников, наступление инвалидизации в результате хронических заболеваний. Органическая природа депрессии отмечается при таких состояниях, как сосудистая мозговая недостаточность, болезнь Паркинсона, БА и многие другие. Депрессия может усугублять имеющиеся когнитивные нарушения или сама по себе быть их причиной (так называемая псевдодеменция). Поэтому коррекция эмоциональных расстройств оказывает благоприятное влияние на когнитивные способности. В терапии депрессии у пожилых лиц следует избегать препаратов с выраженным холинолитическим действием, например, трициклических антидепрессантов, поскольку данные препараты могут усугублять когнитивные расстройства. Напротив, современные антидепрессанты из группы селективных ингибиторов обратного захвата серотонина (флуоксетин, пароксетин, флувоксамин и др.) оказывают положительный эффект в отношении когнитивных функций [3,6,25].
Применение антиоксидантов
Природными антиоксидантами являются витамины С и Е, которые содержатся в продуктах питания. Поэтому предполагается, что диета с высоким содержанием данных витаминов, а также витамина В12 и фолиевой кислоты уменьшает риск возникновения деменции. С этой целью рекомендуется использовать в рационе больше овощей, растительного масла и морепродуктов, а также небольшие (не более 150 г в день) количества красного вина (так называемая среднеземноморская диета). В то же время в ходе Heart Protection Study не удалось продемонстрировать эффективность существующих лекарственных форм витаминов С и Е [27].
Воздействие на нейротрансмиттерные
системы
В лечении деменции наиболее хорошо зарекомендовали себя препараты, модулирующие деятельность церебральных нейротрансмиттерных систем, такие как ингибиторы ацетилхолинэстеразы (ривастигмин, галантамин, ипидакрин) и блокаторы NMDA–рецепторов к глютамату (мемантин). Недавно предпринимались попытки применения ацетилхолинергических препаратов на стадии умеренных когнитивных нарушений, которые, однако, привели к противоречивым результатам. Вероятно, развитие ацетилхолинергического дефицита является достаточно поздним событием патогенеза когнитивных расстройств. Предполагается, что при легких и умеренных когнитивных нарушениях может быть более перспективным воздействие на другие нейротрансмиттерные системы. С этой целью, в частности, используется пирибедил, который сочетает в себе свойства агониста дофаминовых рецепторов и a2–адреноблокатора. Активно изучается также эффективность мемантина на стадии недементных когнитивных нарушений [3–7,21–23].
Вазоактивная терапия
Как при хронической сосудистой мозговой недостаточности, так и при нейродегенеративном процессе патогенетически обоснованной является оптимизация церебральной микроциркуляции с помощью так называемых сосудистых или вазоактивных препаратов.
Сосудистые препараты можно разделить на три основные фармакологические группы:
– ингибиторы фосфодиэстеразы: теофиллин, пентоксифиллин, винпоцетин, препараты гинкго билобы и др. Сосудорасширяющий эффект данных препаратов связан с увеличением в гладкомышечных клетках сосудистой стенки содержания цАМФ, что приводит к их расслаблению и увеличению просвета сосудов. При этом данные препараты оказывают воздействие в основном на сосуды микроциркуляторного русла [3–6];
– блокаторы кальциевых каналов: циннаризин, флунаризин, нимодипин. Указанные препараты оказывают вазодилатирующий эффект благодаря уменьшению внутриклеточного содержания кальция в гладкомышечных клетках сосудистой стенки. По некоторым данным, блокаторы кальциевых каналов оказывают наиболее выраженный эффект на сосуды вертебрально–базилярного бассейна [1,3–6];
– блокаторы a2–адренорецепторов: ницерголин. Данный препарат устраняет сосудосуживающее действие медиаторов симпатической нервной системы – адреналина и норадреналина [3–6].
В настоящее время доказано, что ишемия и гипоксия имеют патогенетическое значение не только при сосудистой мозговой недостаточности, но и при нейродегенеративном процессе. Имеются наблюдения, что длительное (многолетнее) постоянное применение вазоактивных препаратов уменьшает риск перехода легких и умеренных когнитивных нарушений в деменцию [14].
Нейрометаболическая терапия
К настоящему времени накоплен богатый практический опыт применения при легких и умеренных когнитивных нарушениях препаратов, стимулирующих нейрональные метаболические процессы. С этой целью используются производные пирролидона (пирацетам, прамирацетам, анирацетам, карфедон и др.), аминокислотные (глицин, семакс) и пептидергические (Ноопепт, церебролизин и др.) препараты, а также предшественники ацетилхолина.
Точный механизм действия нейрометаболических препаратов пока неизвестен. Однако в эксперименте показано, что под влиянием нейрометаболической терапии в нервных клетках происходит увеличение числа рибосом, интенсифицируется синтез белка, выработка ацетилхолина и других нейротрансмиттеров, что, в конечном итоге, благоприятно влияет на активность нейронов и их способность к установлению новых функциональных связей (так называемая нейрональная пластичность). В клинической практике эффективность нейрометаболической терапии убедительно показано при хронической сосудистой мозговой недостаточности, на начальных стадиях дегенеративного процесса, при возрастном снижении памяти и внимания, а также в восстановительном периоде после острого церебрального повреждение (инсульт, черепно–мозговая травма и др.) [5,6,11,12].
Современным нейрометаболическим препаратом пептидергической природы является Ноопепт (этиловый эфир N–фенил–ацетил–L–пролил–глицина). Данный препарат обладает высокой биодоступностью при пероральном применении и практически не оказывает побочных эффектов. Терапевтическое действие Ноопепта полимодально и складывается из положительного ноотропного, антиамнестического и анксиолитического эффектов. Кроме того, препарат обладает противовоспалительными и иммуномодулирующими свойствами, что имеет большое значение на ранних стадиях нейродегенеративного процесса. Как известно, активация медиаторов тканевого воспаления в паренхиме головного мозга играет важную патогенетическую роль в развитии дегенеративного процесса при БА [8–10].
В эксперименте показано, что на фоне применения Ноопепта улучшается усвоение и воспроизведение информации. В основе данного эффекта лежит оптимизация всех основных этапов мнестической деятельности, таких как обработка информации, консолидация следа памяти, устойчивость мнестического следа по отношению к интерферирующим воздействиям. В клинической практике на фоне терапии Ноопептом отмечено улучшение памяти, внимания и других когнитивных функций у пациентов с цереброваскулярными расстройствами, последствиями черепно–мозговой травмы и хронической алкогольной интоксикацией [2,8–12].
Таким образом, на современном этапе развития неврологии существуют возможности эффективной помощи пациентам с когнитивными нарушениями на всех этапах эволюции когнитивного дефицита. При деменции наиболее хорошо зарекомендовали себя ацетилхолинергические и антиглутаматные препараты. На этапе легких и умеренных когнитивных нарушений приоритетна вазоактивная, нейрометаболическая терапия (Ноопепт), а также влияние на дофаминергическую и норадренергическую систему. Профилактический эффект в отношении возникновения и прогрессирования когнитивных расстройств оказывает контроль сосудистых факторов риска, диета, богатая антиоксидантами, а также высокая интеллектуальная и физическая активность в течение жизни.



Литература
1. Андреев Н.А., Моисеев В.С. Антагонисты кальция в клинической медицине. –М.: РЦ “Фармединфо”, 1995. –161 с.
2. Бобкова, М. А. Грудень, А. Н. Самохин, Н. И. Медвинская, Е. И. Елистратова, L. Morozova–Roch, Т. А. Гудашева, Р. У. Островская, С. Б. Середенин. Ноопепт улучшает пространственную память и стимулирует образование антител к префибриллярной структуре b–амилоида(25–35) у мышей. // Экспериментальная и клиническая фармакология. –2005. –№.5.
3. Гаврилова С.И. Фармакотерапия болезни Альцгеймера. //Москва: изд–во «Пульс». –2003. –115 С.
4. Дамулин И.В. Болезнь Альцгеймера и сосудистая деменция. //Под ред. Н.Н.Яхно. –М. –2002. –С.85.
5. Захаров В.В., И.В.Дамулин, Н.Н.Яхно. Медикаментозная терапия деменций. //Клиническая фармакология и терапия. –1994. –Т.3. –№ 4. –С. 69–75.
6. Захаров В.В., Яхно Н.Н. Нарушения памяти. //Москва: ГеотарМед. –2003. –С.150.
7. Захаров В.В. Всероссийская программа исследований эпидемиологии и терапии когнитивных расстройств в пожилом возрасте («Прометей»). //Неврологический журнал. –2006. –Т.11. –С.27–32.
8. Коваленко Л.П., Н. М. Смольникова, С. В. Алексеева, Е. П. Немова, А. В. Сорокина, М. Г. Мирамедова, С. П. Курапова, Е. И. Сидорина, А. В. Кулакова, Н. О. Даугель–Дауге Доклиническое изучение токсичности Ноопепта. //Экспериментальная и клиническая фармакология. –2002. –№.1.
9. Коваленко Л.П., М. Г. Мирамедова, С. В. Алексеева, Т. А. Гудашева, Р. У. Островская, С. Б. Середенин. Противовоспалительные свойства ноопепта (дипептидного ноотропа ГВС–111). // Экспериментальная и клиническая фармакология №2 – 2002.
10. Молодавкин Г.М., Г. Г. Борликова, Т. А. Воронина, Т. А. Гудашева, Р. У. Островская, Н. А. Тушмалова, С. Б. Середенин. Влияние нового дипептидного ноотропа и его метаболита цикло–L–пролилглицина на транскаллозальный потенциал мозга крыс. //Экспериментальная и клиническая фармакология. –2002. –№.2.
11. Островская Р. У., Гудашева Т. А., Трофимов С. С., Сколдчнов А. П. II Фармакология ноотропов. — М.,–1989. — С. 26–35.
12. Островская Р.У. Ноотропы и нейролептики: есть ли общность в мишенях и нейрорегуляторных механизмах реализации?// Доклад на конгрессе «Человек и лекарство». –2003 г.
13. Яхно Н.Н. Когнитивные расстройства в неврологической клинике. //Неврологический журнал. –2006. –Т.11. –Приложение № 1. –С.4–12.
14. Andrieux S., Amouyal K., Renish W. и соавт. The consumption of vasodilators and Ginkgo biloba (Egb 761) in a population of 7598 women over the age of 75 years. // Research and practice in Alzheimer’s disease. –2001. –V.5. –P.57–68.
15. Barker W.W., Luis C.A., Kashuba A. et al. Relative frequencies of Alzheimer’s disease, Lewy body, vascular and frontotemporal dementia, and hippocampal sclerosis in the State of Florida Brain Bank. //Alzheimer’s Dis Assoc Disord. –2002. –v.16. –P.203–212.
16. DiCarlo A., Baldereschi M., Amaducci L. Et al. Cognitive impairment without dementia in older people: prevalence, vascular risk factors, impact on disability. The Italian Longitudinal Study on Aging. //J Am Ger Soc. –2000. –V.48. –P.775–782.
17. Fu C., Chute D.J., Farag E.S. et al. Comorbidity in dementia: an autopsy study. //Arch Pathol Lab Med. –2004. –V.128. –N.1. –P.32–38.
18. Graham J.E., Rockwood K., Beattie E.L. et al. Prevalence and severity of cognitive impairment with and without dementia in an elderly population. //Lancet. –1997. –V.349. –V.1793–1796.
19. Halama P., G.Bartsch, G.Meng. Hirnleistungstorungen vaskularer Genese. Randomisierte Hullette C.M. Brain banking in the United States. //J Neuropathol Exp Neurol. –2003. –V.62. –N.7. –P.715–722.
20. Knopman D.S., Parisi J.E., Boeve B.F. et al. Vascular dementia in a population–based autopsy study. //Arch Neurol. –2003. –Vol.60. –P.569–575.
21. Knopman D.S. Current treatment of mild cognitive impairment and Alzheimer’s disease. //Curr Neurol Nerosci Rep. –2006. –V.6. –N.5. –P.365–371.
22. Kurshner H.S. Mild cognitive impairment: to treat or not to treat? //Curr Neurol Neurosci Rep. –2005. –V.5. –N.6. –P.455–457.
23. Jelic V., Kivipelto M., Winblad B. Clinical trials in mild cognitive impairment: lessons for the future. //J Neurology Neurosurgery Psychiatry. –2006. –V.77. –N.7. –P.892.
24. Lovenstone S., Gauthier S. Management of dementia. London: Martin Dunitz, 2001.
25. Nolan K.A., Lino M.M., Seligmann A.W., Blass J.P. Absence of vascular dementia in an autopsy series from a dementia clinic. //J Am Geriatr Soc. –1998. –Vol.46. –N.5. –P.597–604.
26. Petersen R. S. Current concepts in mild cognitive impairment // Arch. Neurol. – 2001. – Vol. 58. – P. 1985 – 1992.
27. Skoog I., Gustafson D. Clinical trials for primary prevention in dementia. //In: “Dementia therapeutic research”. K.Rockwood, S.Gauthier (eds). –London a New York: Taylor a Francis. –2006. –P.189–212.
.
Когнитивные нарушения при дисциркуляторной энцефалопатии | Захаров В.В., Локшина А.Б.
Дисциркуляторная энцефалопатия (ДЭ) – это синдром хронического прогрессирующего поражения головного мозга сосудистой этиологии, который развивается в результате повторных острых нарушений мозгового кровообращения и/или хронической недостаточности кровоснабжения головного мозга [3]. Согласно классификации нарушений мозгового кровообращения, принятой в нашей стране, ДЭ является основной клинической формой хронической сосудистой мозговой недостаточности. Данное состояние также обозначается в литературе, как «хроническая ишемия мозга», «ишемическая болезнь мозга», «цереброваскулярная недостаточность» и т.д. С нашей точки зрения, термин «дисциркуляторная энцефалопатия» является наиболее корректным. Он отражает топический диагноз (энцефалопатия) и основной патогенетический механизм формирования синдрома (дисциркуляция, которая включает как хроническую ишемию, так и острые нарушения мозгового кровообращения без клиники инсульта).
Если поражение крупных церебральных артерий обычно приводит к инсультам, то в основе безынсультного формирования синдрома ДЭ в большинстве случаев лежит микроангиопатия. Наиболее частыми ее причинами являются длительно существующая неконтролируемая артериальная гипертензия или сахарный диабет. Реже безынсультное сосудистое поражение головного мозга развивается в результате васкулита, наследственной патологии (например, при синдроме
ЦАДАСИЛ), сенильной амилоидной ангиопатии и др. Сужение церебральных сосудов небольшого калибра приводит к небольшим по размерам (лакунарным) инфарктам мозга, которые часто формируются без клиники инсульта. По статистике на каждый инсульт приходится не менее 1–2 «немых» инфарктов мозга. Не менее часто развиваются микрокровоизлияния, связанные с диапедезным пропитыванием. Они также могут протекать бессимптомно, под маской транзиторной ишемической атаки или малого инсульта. Еще одним характерным морфологическим изменением при ДЭ является лейкоареоз, который представляет собой уменьшение плотности белого вещества. Предполагается, что в основе формирования лейкоареоза лежат повторяющиеся эпизоды кратковременной локальной дисциркуляции, не приводящие к завершенному инфаркту [4,5,23,25,29].
Из–за особенностей кровоснабжения головного мозга излюбленной локализацией лакунарных инфарктов, микрокровоизлияний и лейкоареоза являются подкорковые базальные ганглии и глубинные отделы белого вещества. Данная локализация обусловливает особенности клиники ДЭ, в которой наиболее частый и ранний симптомокомплекс представлен когнитивными нарушениями (КН).
Распространенность КН при ДЭ. КН является одним из основных видов неврологических расстройств при ДЭ. В 1994 году группа авторитетных мировых ангионеврологов предложила термин «сосудистые когнитивные расстройства» (англ. vascular cognitive impairment) для обозначения нарушений высших мозговых функций вследствие цереброваскулярной патологии. Это понятие объединяет как сосудистую деменцию, так и менее тяжелые нарушения когнитивных функций сосудистой этиологии (табл. 1). Подчеркивается, что сосудистые когнитивные нарушения, даже не достигающие выраженности деменции, развиваются в результате длительного течения патологического процесса и знаменуют собой значительное по выраженности цереброваскулярное поражение. Они свидетельствуют о существенном неблагополучии в отношении кровоснабжения головного мозга и поэтому должны рассматриваться в качестве индикатора высокого риска развития инсульта и/или сосудистой деменции [23,24].
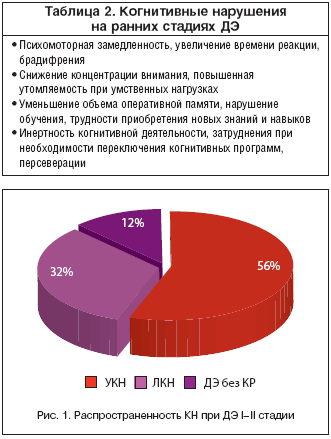
В исследовании, выполненном в клинике нервных болезней им. А.Я. Кожевникова, было показано, что на I и II стадии ДЭ когнитивные нарушения присутствуют в 88% случаев. При этом у 56% обследованных пациентов симптоматика соответствовала общепринятым диагностическим критериям синдрома умеренных когнитивных нарушений [30]. В 32% случаев когнитивные нарушения были легкими по выраженности, то есть присутствовали отдельные когнитивные симптомы, не образующие целостного клинического синдрома [16]. Таким образом, когнитивные нарушения определяются у подавляющего большинства пациентов с ДЭ, причем уже на ранних ее стадиях (рис. 1). Обычно развитие когнитивных нарушений предшествовало формированию других объективных неврологических расстройств, таких как нарушения походки, другие двигательные пирамидные, экстрапирамидные и атактические нарушения. Другими словами, цереброваскулярное заболевание, в том числе достаточно выраженное, может долгое время проявляться только когнитивными расстройствами. Поэтому оценке состояния когнитивной сферы следует уделять особое внимание в диагностике хронической цереброваскулярной недостаточности [13,14].
Клинические особенности КН при ДЭ. Поражение глубинных отделов белого вещества головного мозга ведет к разобщению передних корковых и подкорковых отделов головного мозга с формированием вторичной дисфункции лобных долей головного мозга. Нейропсихологический анализ семиотики когнитивных и других нервно–психических расстройств при ДЭ свидетельствует о лобной дисфункции, как о ведущем патофизиологическом механизме развития данных расстройств. При этом в основе когнитивных нарушений при ДЭ лежит снижение активности психических процессов, трудности переключения когнитивных программ и недостаточность контроля текущей когнитивной деятельности [2,9,11,16,22].
Наиболее ранние когнитивные симптомы ДЭ приведены в таблице 2.
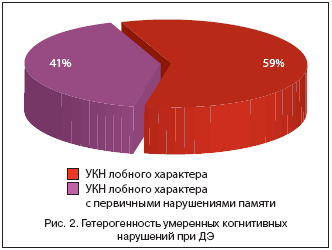
ДЭ сопровождается затруднениями во всех когнитивных сферах, но в наибольшей степени страдают внимание, интеллектуальные операции, пространственный праксис и гнозис. Память в большинстве случаев ДЭ страдает вторично из–за недостаточной активности и избирательности воспроизведения при относительной сохранности запоминания и хранения информации. Однако у части пациентов с ДЭ и умеренными когнитивными нарушениями определяется более выраженное расстройство памяти с признаками первичной недостаточности запоминания поступающей информации (рис. 2). У таких пациентов нейропсихологические методы исследования свидетельствуют о так называемом «гиппокампальном» типе мнестических расстройств: отмечается значительная разница между непосредственным и отсроченным воспроизведением, вплетения постороннего материала, подсказки при воспроизведении малоэффективны [15]. По нашим наблюдениям, «гиппокампальный» тип нарушений памяти является прогностически неблагоприятным признаком в отношении развития деменции. Деменция у таких пациентов носит смешанный (сосудисто–дегенеративный) характер. Таким образом, специфический характер мнестических расстройств может служить ранним признаком присоединения дополнительного дегенеративного процесса.
На стадии сосудистой деменции отмечается выраженное диффузное нарушение всех когнитивных функций, из–за которого пациент лишается независимости и самостоятельности. По данным морфологических методов исследования, на стадии деменции распространенность сопутствующего дегенеративного процесса может достигать более 70% случаев. Вероятно, хроническая сосудистая мозговая недостаточность является фактором риска более раннего начала и быстрого прогрессирования генетически детерминированных форм нейродегенеративных заболеваний. Клинически смешанная (сосудисто–дегенеративная) деменция отличается от «чистой» сосудистой деменции наличием более выраженных нарушений памяти на текущие и отдаленные события жизни, реже – наличием первичных дисфазических расстройств [2,6,20,26].
Взаимосвязь когнитивных и других нервно–психических нарушений при ДЭ. Дисфункция лобных долей головного мозга в результате разобщения корковых и подкорковых церебральных отделов приводит к формированию не только когнитивных, но также эмоциональных и поведенческих нарушений.
Для ранних стадий ДЭ наиболее характерна сосудистая депрессия и эмоциональная лабильность. Снижение фона настроения отмечается в большинстве случаев ДЭ, чаще является легким или умеренным по выраженности. При этом пациенты редко жалуются на снижение фона настроения или подавленность, но обычно предъявляют жалобы соматического характера. Весьма характерны жалобы на головную боль, боли в позвоночнике, суставах, в области внутренних органов, разнообразные неприятные ощущения, не имеющие разумного объяснения с учетом объективного неврологического и соматического статуса. Часто встречаются нарушения сна в виде трудностей засыпания или ранних утренних пробуждений. Напротив, не характерны нарушения пищевого поведения. Сосудистая депрессия обычно сопровождается эмоциональной лабильностью, под которой понимается быстрая смена аффекта, часто в сочетании с повышенной раздражительностью, плаксивостью, обидчивостью по незначительным поводам и др. [2,3,12,28].
Как известно, эмоциональные расстройства могут оказывать неблагоприятное влияние на когнитивную сферу. Однако, по нашим данным, выраженность депрессии при ДЭ не соответствует выраженности когнитивных расстройств. Вероятно, при ДЭ когнитивные и эмоциональные нарушения представляют собой независимые друг от друга, параллельные неврологические расстройства, связанные с дисфункцией передних отделов головного мозга. При этом нарастание лобной дисфункции сопровождается качественной модификацией эмоциональных нарушений с регрессом депрессивного компонента (см. ниже). На стадии легких когнитивных нарушений, по нашим данным, прослеживается обратная корреляция между выраженностью тревоги и когнитивных расстройств. Возможно, активация гипоталамо–гипофизарно–надпочечниковой системы у пациентов с более высоким уровнем тревоги способствует улучшению концентрации внимания и процесса запоминания информации [13–15].
Утяжеление цереброваскулярного поражения головного мозга сопровождается качественной модификацией эмоциональных нарушений. При этом выраженность сосудистой депрессии уменьшается, и, напротив, появляются и нарастают признаки апатии, снижается мотивация и инициатива, формируется безразличие к себе и окружающим [12,28]. Дифференциальный диагноз между апатией и депрессией может представлять значительные затруднения, особенно у пациентов с выраженными когнитивными нарушениями. Как при депрессии, так и при апатии значительно уменьшаются побуждения к какой–либо деятельности, пациенты большую часть времени ничем не заняты. Однако при депрессии бездеятельность сопровождается неприятным эмоциональным переживанием и внутренним страданием пациента – в отличие от апатии, при которой больные эмоционально безучастны, а переживания отсутствуют или носят формальный характер.
Апатия и снижение инициативы обычно сочетаются с сосудистой деменцией, в то время как депрессия и эмоциональная лабильность отмечаются у пациентов с легкими и умеренными когнитивными нарушениями.
Диагностика КН при ДЭ. Как уже указывалось выше, когнитивные и другие нервно–психические нарушения представляют собой наиболее распространенный и ранний признак ДЭ. Поэтому для своевременной диагностики цереброваскулярной недостаточности необходима адекватная оценка нервно–психической сферы. Наиболее актуальным является исследование состояния когнитивной сферы у пациентов пожилого возраста при наличии жалоб когнитивного характера (снижение памяти, повышенная утомляемость при умственных нагрузках) и при наличии сердечно–сосудистых заболеваний, таких как гипертоническая болезнь, атеросклероз церебральных артерий, сахарный диабет и др.
Для оценки состояния когнитивных функций используется нейропсихологический метод исследования. В повседневной клинической практике используются так называемые скрининговые психометрические шкалы, которые представляют собой набор наиболее простых проб на различные аспекты когнитивной деятельности: память, внимание, интеллект, праксис, гнозис, речь, ориентировку и т. д. Общепринятым стандартом скрининга когнитивных нарушений является тестирование по краткой шкале оценки психического статуса (КШОПС) [21]. Однако следует иметь в виду, что данная методика была изначально разработана для диагностики болезни Альцгеймера. Задания, включенные в данную методику, оценивают функции задних отделов коры головного мозга, такие как память, ориентировка, счет, речь и конструктивный праксис. Пациенты с ДЭ, даже при значительной выраженности когнитивных нарушений, могут получить по КШОПС высокий балл, так как при ДЭ преимущественно страдают передние отделы головного мозга. Поэтому у пациентов с сопутствующими сердечно–сосудистыми заболеваниями целесообразно использовать нейропсихологические тесты, чувствительные к лобной дисфункции. Такими методиками являются, в частности, тест рисования часов и батарея лобных тестов B. Dubois (табл. 3 [17,28]). Смешанная (сосудисто–дегенеративная) деменция характеризуется наличием как когнитивных симптомов лобной дисфункции, так и заинтересованности височно–теменных отделов головного мозга [6].
Ведение пациентов с ДЭ и когнитивными нарушениями. Лечение сосудистых когнитивных нарушений в первую очередь должно быть направлено на их причину, то есть на основное сосудистое заболевание, обусловливающее ДЭ. Актуальность этого положения подчеркивается тем, что сосудистые когнитивные нарушения рассматриваются сегодня в качестве индикатора высокого риска развития инсульта. Поэтому установление диагноза сосудистых когнитивных нарушений должно неизбежно повлечь за собой всестороннюю оценку состояния сердечно–сосудистой системы и коррекцию модифицируемых факторов риска церебральной ишемии. Указанные мероприятия важны для профилактики инсульта, сосудистой и смешанной деменции.
Наиболее частыми причинами ДЭ являются артериальная гипертензия, диабетическая микроангиопатия, атеросклероз магистральных артерий головы и заболевания сердца с повышенным риском тромбоэмболии в головной мозг. При наличии артериальной гипертензии у пациентов без гемодинамически значимых артериальных стенозов следует стремиться к достижению нормотонии (АД не выше 140/90). Однако контроль артериальной гипертензии должен осуществляться постепенно (чрезмерно быстрое снижение АД может приводить к усугублению церебральной ишемии). До сих пор не решен вопрос о целевых цифрах АД у пациентов с гемодинамически значимыми стенозами (более 70% просвета сосуда) магистральных артерий головы. Вероятно, стремиться к полному контролю артериальной гипертензии в этих случаях не следует [1,3,22].
Атеросклероз магистральных артерий головы является показанием для назначения антиагрегантов: ацетилсалициловой кислоты (50–150 мг в сутки) или клопидогрела в дозе 75 мг в сутки. К препаратам с антиагрегантными свойствами относится также дипиридомол. Монотерапия данным препаратом не оказывает убедительного антиагрегантного эффекта, однако присоединение дипиридомола усиливает антиагрегантный эффект ацетилсалициловой кислоты [1,3].
При наличии мерцательной аритмии предсердий, клапанных пороков, а также при кардиоэмболических инсультах в анамнезе эффективность антиагрегантной терапии недостаточна. В этих случаях для уменьшения риска повторной тромбоэмболии в головной мозг показано применение непрямых антикоагулянтов. Препаратом выбора является варфарин. Терапию данным препаратом необходимо проводить под регулярным контролем международного нормализованного отношения [1,3].
Важным фактором риска церебральной ишемии является гиперлипидемия. Пациентам с ДЭ необходимо регулярно выполнять исследования липидного профиля и при наличии гиперлипидемии следует назначать гиполипидемические препараты. Дополнительными показаниями к гиполипидемической терапии являются наличие артериальных стенозов, ишемической болезни сердца и сахарного диабета. Наиболее перспективно назначение препаратов из группы статинов (ловастатин, симвастатин, аторвастатин и др.). В настоящее время предполагается и активно изучается эффективность статинов не только в отношении коррекции липидного обмена, но и профилактическое действие данного класса препаратов в отношении нейродегенеративного процесса, который нередко развивается на фоне хронической сосудистой мозговой недостаточности [1,31,32].
Патогенетически обоснованными мероприятиями является также воздействие на другие корригируемые факторы риска ишемии головного мозга. К таким факторам относятся курение, сахарный диабет, ожирение, гиподинамия и др. [1,3].
У пациентов с ДЭ широко применяются вазоактивные препараты, которые, как предполагается, воздействуют преимущественно на микроциркуляторное русло, не вызывая эффекта «обкрадывания». К таким препаратам относятся ингибиторы фосфодиэстеразы (пентоксифиллин, винпоцетин, препараты гингко билобы), блокаторы кальциевых каналов (циннаризин, нимодипин), альфа–адреноблокаторы (ницерголин, пирибедил) и некоторые другие лекарственные средства [2,3,9].
Другой подход к патогенетической терапии сосудистых когнитивных нарушений – обеспечение метаболической защиты нейронов головного мозга от ишемии и гипоксии. С этой целью используют нейрометаболические препараты, которые повышают выживаемость нейронов при различных патологических состояниях, воздействуя на непосредственные механизмы церебрального повреждения (процессы перекисного окисления липидов, эксайтотоксичность и др.). Помимо нейропротективного эффекта, нейрометаболическая терапия способствует также оптимизации репаративных процессов головного мозга в восстановительном периоде после острого церебрального повреждения. Поэтому нейрометаболическая терапия используется как при хронической мозговой недостаточности, так и в восстановительном периоде инсульта. К препаратам нейрометаболического действия относятся производные пирролидона (пирацетам и др.), пептидергические и аминокислотные препараты (актовегин, церебролизин, кортексин, семакс), предшественники нейромедиаторов (холина альфосцерат) [2,3,8,9].
В отечественной неврологической практике традиционно принято курсовое назначение вазоактивных и нейрометаболических препаратов: по 2–3 месяца 1–2 курса в год. Патогенетически обоснованным является также более длительный прием препаратов данной группы при ДЭ (до 6–12 месяцев). Допустимо и оправдано одновременное назначение вазоактивного и метаболического препарата.
Многочисленные исследования свидетельствуют, что нейрохимической основой сосудистых когнитивных нарушений является ацетилхолинергическая недостаточность. Причиной ее возникновения при ДЭ является ишемическое поражение перивентрикулярного белого вещества, в котором проходят, в том числе, ацетилхолинергические аксоны. Следует отметить, что ацетилхолинергическая недостаточность закономерно развивается также при наиболее распространенных формах дегенеративной деменции – болезни Альцгеймера и деменции с тельцами Леви. Поэтому препараты с ацетилхолинергическими свойствами показаны при наличии когнитивных нарушений как дегенеративной, так и сосудистой этиологии и смешанной (сосудисто–дегенеративной) этиологии [9,18,19,22,27,28].
Центральным ацетилхолинергическим эффектом обладает нейрометаболический препарат холина альфосцерат. Применение данного препарата способствует увеличению синтеза ацетилхолина и повышению активности церебральной ацетилхолинергической системы. Благодаря указанным свойствам холина альфосцерат успешно применятся для патогенетической терапии когнитивных нарушений при сосудистой патологии головного мозга. На фоне применения данного препарата отмечается улучшение запоминания и воспроизведения информации, повышение концентрации внимания, умственной работоспособности. Препарат также способствует регрессу эмоциональных расстройств и повышению функциональной адаптации пациентов с ДЭ. Помимо ацетилхолинергического эффекта, холина альфосцерат, будучи предшественником фосфатидилхолина, оказывает мембраностабилизирующий эффект. С данным фармакологическим свойством препарата связано его нейропротективное действие в условиях ишемии и гипоксии, а также при других патологических состояниях [7,8,10].
На стадии сосудистой и смешанной деменции с симптоматической целью успешно применяются ингибиторы центральной ацетилхолинэстеразы (галантамин, ривастигмин, ипидакрин) и обратимый блокатор НМДА–рецепторов мемантин [19,27,28].
При сосудистой депрессии используются антидепрессанты, не обладающие центральным холинолитическим эффектом (селективные ингибиторы обратного захвата серотонина, селективные ингибиторы обратного захвата серотонина и норадреналина) [28].
Таким образом, когнитивные нарушения являются важной составной частью синдрома ДЭ. Диагностика сосудистых когнитивных нарушений имеет большое значение для правильной оценки неврологического статуса, синдромального, топического и нозологического диагноза. Тактика ведения пациентов с ДЭ и когнитивными нарушениями должна включать воздействие на этиологические основы ДЭ, то есть на основное сосудистое заболевание, патогенетические механизмы ДЭ и имеющиеся симптомы. На фоне адекватной терапии можно значительно уменьшить риск развития повторных острых нарушений мозгового кровообращения и трансформации легких и умеренных когнитивных нарушений в деменцию. Важной задачей врача является также повышение качества жизни пациентов и их родственников.


Литература
1. Варлоу Ч.П., М.С.Деннис, Ж.ван Гейн и др. Инсульт. Практическое руководство для ведения больных //Пер. с англ. –СПб. –1998. –С.629
2. Дамулин И.В. Болезнь Альцгеймера и сосудистая деменция. //Под ред. Н.Н.Яхно. –М. –2002. –С.85.
3. Дамулин И.В., Парфенов В.А., Скоромец А.А., Н.Н.Яхно. Нарушения кровообращения в головном и спинном мозге. //В кн.: «Болезни нервной системы. Руководство для врачей». Н.Н.Яхно, Д.Р.Штульман (ред.). –М.: «Медицина». –2005. –С.231–302.
4. Левин О.С., Дамулин И.В. Диффузные изменения белого вещества (лейкоареоз) и проблема сосудистой деменции. //В кн.: «Достижения в нейрогериатрии». Под ред. Н.Н.Яхно, И.В.Дамулина. –М.: изд–во ММА. –1995. –С.189–231.
5. Мартынов А.И., Шмырев В.И., Остроумова О.Д. и соавт. Особенности поражения белого вещества головного мозга у пожилых больных с артериальной гипертензией. //Клиническая медицина. –2000. –№ 6. –С.11–15.
6. Мхитарян Э.А. Преображенская И.С. Болезнь Альцгеймера и цереброваскулярные расстройства.//Неврол. журнал (Приложение). –2006. –№1. –с.4–12.
7. Одинак М.М., Вознюк И.А. Современные средства лечения ишемического инсульта. //Терра–Медика –1999. № 2. –С.28–36.
8. Парфенов В.А. Метаболическая терапия ишемического инсульта. //Русский медицинский журнал. –2002. –Т.10. № 25. –С.21–30.
9. Преображенская И.С., Яхно Н.Н. Сосудистые когнитивные нарушения: клинические проявления, диагностика, лечение.// Неврологический журнал. –2007. –Т.12. –№5. –С.45–50.
10. Селезнева Н.Д., Колыхалов И.В., Герасимов Н.П.,Жариков Г.А.Гаврилова С.И. Применение глиатилина для лечения деменций альцгеймеровского типа. //Социальная и клиническая Психиатрия. –1998. № 4. –С.42–51.
11. Яхно Н.Н., Левин О.С., Дамулин И.В. Сопоставление клинических и МРТ–данных при дисциркуляторной энцефалопатии. Сообщение 2: когнитивные нарушения. //Неврол.журн. –2001. –Т.6, № 3. –С.10–19.
12. Яхно Н.Н., В.В.Захаров. Когнитивные и эмоционально–аффективные нарушения при дисциркуляторной энцефалопатии. //Русский медицинский журнал. –2002. –Т.10. № 12–13. –С.539–542.
13. Яхно Н.Н., Локшина А.Б., Захаров В.В. Легкие и умеренные когнитивные расстройства при дисциркуляторной энцефалопатии. //Неврологический журнал. –2004. –№2. –С.30–35.
14. Яхно Н.Н., Локшина А.Б., Захаров В.В. Легкие и умеренные когнитивные расстройства при дисциркуляторной энцефалопатии. //Клиническая геронтология. –2005. –Т.11. –№ 9. –С.38–39.
15. Яхно Н.Н., Захаров В.В., Локшина А.Б. Синдром умеренных когнитивных нарушений при дисциркуляторной энцефалопатии. //Журнал неврол. и психиатр. им. С.С.Корсакова. –2005. –Т.105. –№ 2. –С.13–17.
16. Яхно Н.Н. Когнитивные расстройства в неврологической клинике. //Неврологический журнал. –2006. –Т.11. –Приложение № 1. –С.4–12.
17. Dubois B., A.Slachevsky, I.Litvan, B.Pillon. The FAB: a frontal assessement battery at bedside. //Neurology. –2000. –V.55. –P.1621–1626.
18. Erkinjuntti T., Roman G., Gauthier S. et al. Emerging therapies for vascular dementia and vascular cognitive impairment. //Stroke. –2004. –Vol.35. P.1010–1017.
19. Erkinjuntti T., Roman G., Gauthier S. Treatment of vascular dementia–evidence from clinical trials with cholinesterase inhibitors. //J Neurol Sci. –2004. –Vol.226. –P.63–66.
20. Fu C., Chute D.J., Farag E.S. et al. Comorbidity in dementia: an autopsy study. //Arch Pathol Lab Med. –2004. –V.128. –N.1. –P.32–38.
21. Folstein M.F., S.E.Folstein, McHugh P.R. Mini–Mental State: a practical guide for grading the mental state of patients for the clinician. J Psych Res, 1975, V.12, pp 189–198.
22. Golomb J., Kluger A., Garrard P., Ferris S. Clinician’s manual on mild cognitive impairment // London: Science Press, 2001.
23. Hachinski V.C., Lassen N.A., Marshall Y. Multi–infarct dementia: a cause of mental deterioration in the elderly. //Lancet. –1974. –V.2. –P.207.
24. Hachinski V. Vascular dementia: radical re–definition. In Vascular dementia: ethiology, pathogenesis and clinical aspects. //Ed. By L.A.Carlson, S.G.Gottfries, B.Winblad. –Basel ETC: S.Karger. –1994. –P.2–4.
25. Hershey L.A., Olszewski W.A. Ischemic vascular dementia. //In: Handbook of Demented Illnesses. Ed. by J.C.Morris. –New York etc.: Marcel Dekker, Inc. –1994. –P.335–351
26. Korczyn A. D. Mixed Dementia—the Most Common Cause of Dementia / Ann. N.Y. Acad. Sci. – 2002. – V.977. – P.129–134.
27. Kumar V., Messina J., Hartman R., Cicin–Sain A. Presence of vascular risk factors in AD patients predicts greater response to cholinesterase inhibition. //Neurobiol. Aging. –2000. –Vol.21. –N.1S. –P.S218.
28. Lovenstone S., Gauthier S. Management of dementia. //London: Martin Dunitz, 2001.
29. Pantoni L., Garsia J. Pathogenesis of leukoaraiosis. //Stroke. –1997. –V.28. –P.652–659.
30. Petersen R.S., Touchon J. Consensus on mild cognitive impairment. //Research and practice in AD. EADS–ADCS joint meeting. –2005. –V.10. –P.24–32.
31. Simon M., Keller P., DeStrooper B. et al. Cholesterol depletion inhibits the generation of beta–amyloid in hippocampal neurons. //Proc Natl Acad Sci USA. –1998. –V.95. –P.6460–6464.
32. Shepherd J., Blauw G., Murphy M. et al. Pravastatin in elderly individuals at risk of vascular disease (PROSPER): a randomized placebo controlled trial. //Lancet. –2002. –V.360. –P.1623–1630.
.
Когнитивный и нейросенсорный дефицит у взрослых и детей
 Когнитивный дефицит у взрослых считается одним из самых распространенных неврологических симптомов, указывающих на нарушение в функционировании мозга. Это сказывается на том, как человек воспринимает мир вокруг себя, и нарушает его повседневную жизнь, мешая познавательной деятельности.
Когнитивный дефицит у взрослых считается одним из самых распространенных неврологических симптомов, указывающих на нарушение в функционировании мозга. Это сказывается на том, как человек воспринимает мир вокруг себя, и нарушает его повседневную жизнь, мешая познавательной деятельности.
Типы когнитивной деятельности
Когнитивный и нейросенсорный дефицит – эти термины являются синонимами. Они объединяют нарушения, затрагивающие пять типов познавательной работы мозга в одну большую группу:
- Память, то есть, навык усвоения полученной информации, сохранение ее и повторение в соответствующих ситуациях.
- Гнозис, отвечающий за то, чтобы человек мог воспринимать информацию, получаемую от мира. Выражается в виде способности к ее анализу и формированию соответствующих ощущений, идущих от органов чувств.
- Речь, иначе говоря – это возможность человека проводить обмен информацией через высказывания.
- Праксис или способность к получению, сохранению и дальнейшему применению моторных навыков.
- Интеллект, то есть, умение сопоставлять поступающую информацию, искать схожее и различное в ней.
Любые нарушения в познавательной деятельности затрудняют или делают невозможным нормальное восприятие окружающего мира, происходящих вокруг человека событий, а также поддержание прежней активности в социальной и профессиональной сфере.
Узнайте о причинах демиелинизирующих заболеваний головного мозга: симптомы и лечение.
Читайте про когнитивные функции их связь с отделами мозга и причины нарушения.
Почему развивается когнитивная дисфункция
Этиологические факторы возникновения познавательных расстройств классифицируют на две группы: функциональные, которые также называются временными, и органические, спровоцированные определенной патологией в мозге.
Функциональные факторы
Временные нарушения познавательной сферы не связаны с изменениями в структурах мозга и потому не носят постоянный характер. Этиологическими факторами этой группы считаются: психоэмоциональное перенапряжение, длительное воздействие стресса, физические перегрузки и накопление большого количества негативных эмоций.
Когнитивный дефицит этой группы может развиться в любом возрасте и не считается опасным для человека. Симптомы нарушений становятся менее выраженными или полностью проходят после устранения причины проблемы.
Органические патологии
Когнитивные расстройства органической природы более характерны для взрослого населения и могут быть вызваны нарушенным кровоснабжением мозга, черепно-мозговыми травмами, метаболическими или возрастными изменениями.
К числу причин когнитивного дефицита из-за нарушенного кровоснабжения относятся:
- Гипертония.
- Атеросклероз сосудов.
- Патологии сердечно-сосудистой системы вроде ишемической болезни сердца или инфаркта.
- Инсульты.
 Патологические нарушения в метаболизме вызываются:
Патологические нарушения в метаболизме вызываются:
- эндокринными заболеваниями: гипотиреозом и сахарным диабетом;
- недостаточностью почек или печени;
- сниженным поступлением или неполным усвоением витамина В12 и фолиевой кислоты;
- частым употреблением алкоголя;
- курением;
- приемом наркотиков и отдельных лекарств.
Возрастные изменения мозга вызваны атрофией, причинами развития которой могут быть болезнь Альцгеймера или синдром Паркинсона.
Степени когнитивной дисфункции
Существуют 3 степени нарушения познавательной сферы у человека:
- Легкая.
- Умеренная.
- Тяжелая.
Для легкой фазы характерна незначительно выраженная симптоматика в виде сниженной способности к концентрации внимания, небольшого ухудшения работы памяти, повышение утомляемости от умственной деятельности. В таком состоянии человек способен забыть имя знакомого, у него затруднена ориентация в незнакомых местах, возникают сложности в подборе подходящих слов. Часто наблюдается забывчивость. Пациент не помнит, где был оставлен им какой-то предмет.
Умеренные нарушения сопровождаются ухудшением одной или нескольких функций мозга. При этом человек нуждается в помощи окружающих, так как не может вспомнить некоторые моменты жизни и не способен ориентироваться даже в знакомых местах.
Тяжелую степень когнитивной дисфункции называют деменцией. Для нее характерно развитие проблем не только в работе и социальной сфере, но и в способности к самообслуживанию. Человек нуждается в постоянной помощи близких. Он дезориентирован во времени, не способен вспомнить многие промежутки своей жизни. Это может сопровождаться развитием каких-либо навязчивых идей, повышением тревожности, бредом или появлением галлюцинаций.
Когнитивный дефицит у детей встречается нередко при гиповитаминозе. Причинами могут стать также внутриутробные инфекции, гипоксия плода и травмы, полученные во время прохождения ребенком родовых путей матери. Типичными признаками нарушения когнитивных функций выступают: синдром гиперактивности и дефицита внимания, затруднения при обучении речи и письму, расстройства моторных процессов и поведенческой сферы.
Читайте про проявления нарушений когнитивных функций у детей и способы лечения расстройства.
Все про болезнь Фара: причины, симптомы, диагностика и терапия.
Узнайте про транскраниальную микрополяризацию головного мозга и показания к проведению процедуры.
Лечение познавательных нарушений
Когнитивный дефицит у взрослых требует лечения, которое должен назначить невропатолог. В соответствии с причинами нарушений врач может прибегнуть к направлению пациента к психологу, психиатру или логопеду, на физиотерапию, а также использовать лекарственные средства.
В медикаментозной терапии могут применяться:
- Ноотропы (Пирацетам).
- Лекарства, влияющие на метаболизм в головном мозге (Глицин).
- Нейропротекторы (Церебролизин).
- Препараты для борьбы с деменцией (Мемантин).
- Средства, направленные на коррекцию гиперхолестеринемии (Торвакард).
Когнитивная дисфункция представляет собой серьезную проблему, существенно влияющую на жизнь человека. Потому максимально раннее выявление развивающегося синдрома необходимо для быстрого формирования соответствующей схемы лечения и повышения шансов на сохранение привычной жизнедеятельности.
 Загрузка…
Загрузка…
Снижение рабочей памяти и исполнительных функций при нормальном старении, легком когнитивном нарушении и болезни Альцгеймера
Болезнь Альцгеймера (БА) — прогрессирующее нейродегенеративное заболевание, характеризующееся дефицитом эпизодической памяти, рабочей памяти (WM) и исполнительной функции. Примеры исполнительной дисфункции при БА включают плохое избирательное и разделенное внимание, неудачное подавление мешающих стимулов и плохие навыки манипуляции. Хотя эпизодические дефициты во время прогрессирования заболевания широко изучались и являются эталоном вероятного диагноза БА, в более поздних исследованиях изучались СМ и снижение управляющих функций во время умеренного когнитивного нарушения (MCI), также называемого доклинической стадией БА.MCI — критический период, в течение которого все еще происходят когнитивная реструктуризация и нейропластичность, такая как компенсация; следовательно, когнитивные методы лечения могут иметь положительный эффект на снижение вероятности прогрессирования AD во время MCI. Мониторинг выполнения задач рабочей памяти и исполнительных функций для отслеживания когнитивных функций может сигнализировать о переходе от нормального познания к MCI к AD. В настоящем обзоре отслеживается снижение WM в результате нормального старения, MCI и AD, чтобы выделить поведенческие и неврологические различия, которые различают эти три стадии, чтобы направить будущие исследования по диагностике MCI, когнитивной терапии и профилактике AD.
1. Введение
Болезнь Альцгеймера (БА) является шестой ведущей причиной смерти в Соединенных Штатах и пятой ведущей причиной смерти среди людей старше 65 лет, как это определено Центром по контролю заболеваний [1]. Риск развития БА с возрастом увеличивается экспоненциально [2]. В настоящее время верификация диагноза БА осуществляется путем посмертного выявления патологии в нервной ткани, в частности внеклеточных амилоидных бляшек и внутриклеточных нейрофибриллярных клубков тау; однако когнитивные изменения заметны на ранних стадиях патогенеза БА и умеренного когнитивного нарушения (MCI).В следующем обзоре исследуется обнаружение дефицита рабочей памяти (WM) посредством поведенческих, функциональных и структурных изменений у взрослых без нарушений, MCI и AD. Мы дополнительно исследуем, может ли отслеживание WM и навыков управляющих функций с течением времени, в дополнение к анализу биомаркеров, идентифицировать людей во время MCI как подверженных риску прогрессирования в сторону AD.
2. Отслеживание снижения до и после начала AD
От 10 до 20 процентов взрослых старше 65 лет имеют диагноз MCI [3–5], и примерно у 10 процентов взрослых MCI развивается AD [6] .По сравнению с здоровыми взрослыми того же возраста, у людей с MCI, как правило, быстрее развивается AD [7]. Невропатологически взрослые с MCI обнаруживают амилоидные бляшки и нейрофибриллярные тау-сплетения в уязвимых для AD областях мозга, ответственных за эпизодическую память, особенно в обонятельной коре, субикулуме и парагиппокампальной извилине в медиальных височных долях [8, 9], хотя и в меньшей степени. степени по сравнению с мозгом пациента с БА [10].
Поведенческие исследования показывают, что у взрослых с MCI наблюдается когнитивный дефицит в отношении WM, центральной исполнительной функции и ресурсов внимания по сравнению с контрольной группой без нарушений соответствующего возраста [11–15].Доклинические пациенты сами сообщают о субъективном снижении когнитивных функций до того, как они обнаружат нарушение при оценке когнитивных функций [16]. В то время как нарушения WM во время MCI не поддаются измеримому вмешательству в повседневную деятельность, они более серьезны, чем дефициты WM, возникающие в результате нормального старения. Хотя эти нарушения не связаны с эпизодической памятью, они могут надежно предсказать прогрессирование от MCI к AD [16, 17], особенно в сочетании с дефицитом эпизодической памяти [13, 15]. Взятые вместе, результаты невропатологии и когнитивных нарушений предполагают, что диагноз БА может быть основан на континууме, который начинается как MCI и переходит в AD, хотя могут быть более тонкие признаки до диагностики MCI.
Эти наблюдения вызывают два вопроса без ответа: (1) Какие различия существуют между когнитивно нормальными взрослыми с MCI и AD в отношении нейронной активации и привлечения ресурсов WM ? и (2) , что эти различия могут сказать нам о вероятности прогрессирования человека до MCI или AD? Исследования показывают, что существует большой потенциал для устранения когнитивного дефицита и усиления исполнительной функции на стадии MCI [18]. Сообщается, что взрослые с MCI восстанавливают когнитивные функции, занимаясь физическими упражнениями [19], употребляя здоровую пищу (например,g., рыбий жир) [20], снижение потребления холестерина ЛПНП [21] и выполнение сложных когнитивных задач [22]. Таким образом, клинические инструменты, которые точно определяют прогрессирование от нормального когнитивного старения к MCI, дают доклиническим взрослым возможность активно участвовать в задачах, которые могут помочь улучшить и сохранить их когнитивные функции.
3. Рабочая память: краткий обзор
WM — это система, которая поддерживает когнитивные действия, начиная от распределения внимания до конкретных стимулов (т.е. избирательное внимание) к принятию сложных решений [23]. В частности, WM способствует активному краткосрочному хранению информации для последующего доступа и манипуляции [24]. Форма информации, хранящейся в WM, является слуховой, что поддерживается фонологической петлей (например, для продвижения языка
.
Список лекарств для легких когнитивных нарушений (1 в сравнении)
Другие названия:
MCI; Потеря памяти
О легких когнитивных нарушениях: Легкие когнитивные нарушения (MCI) — это общий термин, чаще всего определяемый как тонкое, но измеримое нарушение памяти. MCI характеризуется постоянными проблемами с памятью, но не спутанностью сознания, проблемами внимания или языковыми трудностями.
Используемые наркотики
для лечения легких когнитивных нарушений
Следующий список лекарств так или иначе связан с
используется при лечении этого состояния.
Альтернативные методы лечения легких когнитивных нарушений
Следующие продукты считаются альтернативными методами лечения
или натуральные средства от легких когнитивных нарушений. Их
эффективность не могла быть научно проверена в той же степени
как препараты, перечисленные в таблице выше. Однако могут быть исторические,
культурные или анекдотические данные, связывающие их использование с лечением
Легкие когнитивные нарушения.
Подробнее о легких когнитивных нарушениях
Клинические коды МКБ-10 CM (внешние)
Легенда
| Rx | Только по рецепту |
|---|---|
| ОТС | Без рецепта |
| Rx / OTC | По рецепту или без рецепта |
| Не этикетка | Это лекарство не может быть одобрено FDA для лечения этого состояния. |
| Категория беременности | |
|---|---|
| А | Адекватные и хорошо контролируемые исследования не смогли продемонстрировать риск для плода в первом триместре беременности (и нет доказательств риска в более поздних триместрах). |
| B | Исследования воспроизводства животных не смогли продемонстрировать риск для плода, и нет адекватных и хорошо контролируемых исследований у беременных женщин. |
| С | Исследования репродукции животных показали неблагоприятное воздействие на плод, и нет адекватных и хорошо контролируемых исследований на людях, но потенциальные преимущества могут оправдывать использование у беременных женщин, несмотря на потенциальные риски. |
| D | Имеются положительные доказательства риска для плода человека, основанные на данных о побочных реакциях, полученных в результате исследований или маркетингового опыта или исследований на людях, но потенциальные преимущества могут потребовать применения у беременных женщин, несмотря на потенциальные риски. |
| х | Исследования на животных или людях продемонстрировали аномалии развития плода и / или есть положительные доказательства риска для плода у человека, основанные на данных о побочных реакциях из исследовательского или маркетингового опыта, и риски, связанные с использованием у беременных женщин, явно перевешивают потенциальную пользу. |
| N | FDA не классифицировало препарат. |
| Закон о контролируемых веществах (CSA) Приложение | |
|---|---|
| N | Не подпадает под действие Закона о контролируемых веществах. |
| 1 | Имеет высокий потенциал для злоупотреблений. В настоящее время не применяется в медицинских целях в США. Отсутствуют общепринятые правила безопасности для использования под медицинским наблюдением. |
| 2 | Имеет высокий потенциал для злоупотреблений. В настоящее время разрешено медицинское использование для лечения в Соединенных Штатах или в настоящее время принятое медицинское использование с серьезными ограничениями. Жестокое обращение может привести к серьезной психологической или физической зависимости. |
| 3 | Имеет меньшую вероятность злоупотребления, чем те, которые указаны в таблицах 1 и 2. В настоящее время разрешено медицинское использование для лечения в США. Злоупотребление может привести к умеренной или низкой физической зависимости или высокой психологической зависимости. |
| 4 | Имеет низкий потенциал злоупотребления по сравнению с теми, которые указаны в списке 3. В настоящее время он признан в медицине для лечения в Соединенных Штатах. Злоупотребление может привести к ограниченной физической или психологической зависимости по сравнению с теми, которые указаны в Таблице 3. |
| 5 | Имеет низкий потенциал злоупотребления по сравнению с теми, которые указаны в таблице 4. В настоящее время разрешено медицинское использование в лечении в Соединенных Штатах. Злоупотребление может привести к ограниченной физической или психологической зависимости по сравнению с теми, которые указаны в таблице 4. |
| Спирт | |
|---|---|
| х | Взаимодействует с алкоголем. |
Дополнительная информация
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, отображаемая на этой странице, применима к вашим личным обстоятельствам.
Заявление об отказе от ответственности за медицинское обслуживание
.

 Узнайте о причинах демиелинизирующих заболеваний головного мозга: симптомы и лечение.
Узнайте о причинах демиелинизирующих заболеваний головного мозга: симптомы и лечение. Читайте про проявления нарушений когнитивных функций у детей и способы лечения расстройства.
Читайте про проявления нарушений когнитивных функций у детей и способы лечения расстройства.